유방 절제 뒤 재건이나 미용 목적의 인공유방 보형물은 국내에서 가장 많이 시술되는 인체이식형 의료기기다.
또한 식품의약품안전처가 지정한 추적관리대상 의료기기 52개 품목 가운데 부작용 사례가 가장 많이 발생한 품목이기도 하다. 추적관리대상 의료기기는 인체에 1년 이상 이식되는 의료기기다.
뉴스타파가 국회 보건복지위원회 윤일규 의원실을 통해 입수한 식약처 자료에 따르면 지난 5년 동안 식약처에 보고된 추적관리대상 인체이식 의료기기 부작용 사례 4,884건 가운데 88%가 넘는 4,324건이 실리콘겔 인공유방 제품에서 일어났다.
또 이 이상 사례 4,324건 가운데 98%에 이르는 4,240건이 글로벌 의료기기 제조사 엘러간(2,411건)과 존슨앤드존슨메디칼의 유방보형물 브랜드 멘토(1,830건) 등 두 업체 제품에서 발생했다. 주요 이상 사례 유형은 보형물 주변에 피막이 형성돼 딱딱하게 되는 구형구축과 파열이다.

이 두 업체는 지난 4년 동안 국내 병원에 총 100,213개의 인공유방 보형물을 납품한 것으로 나타났다. 연평균 2만여 명에게 시술할 수 있는 물량이다. 하지만 제조회사는 부작용에 대해 별다른 조치를 취하지 않고 있고, 식약처 또한 사실상 손을 놓고 있다.
뉴스타파 취재진이 입수한 식약처의 추적관리대상 의료기기의 ‘심각한 이상사례’ 보고서에서도 인공유방 관련 이상사례가 확인된다.
2017년 00일 작성된 보고서에 따르면 46세 C씨는 지난 2012년 유방암 진단을 받고 유방절제술 이후 가슴 재건을 위해 엘러간의 실리콘 인공유방 보형물 제품(실리콘겔인공유방 모델명 ‘115-290’, 수허 07-634호)을 이식받았다.
하지만 시술 4년 반 뒤 보형물 파열이 의심돼 병원을 찾았다. 이미 실리콘은 누출돼 있었고, 부작용으로 실리콘 육아종과 염증이 형성된 상태였다.
역시 2017년 작성된 한 보고서를 보면 47세 K씨도 2013년 유방암 진단으로 종양을 절제하고 재건 시술을 받았다. K씨도 엘러간의 실리콘 제품(실리콘겔인공유방 모델명 ‘N-27-MF115-255’, 수허 12-940호)을 이식받았는데, 시술 4년 뒤 제품이 파열돼 실리콘 누출이 발견됐다. 다행히 합병증은 없었지만 다시 유방재건술을 받아야 했다.
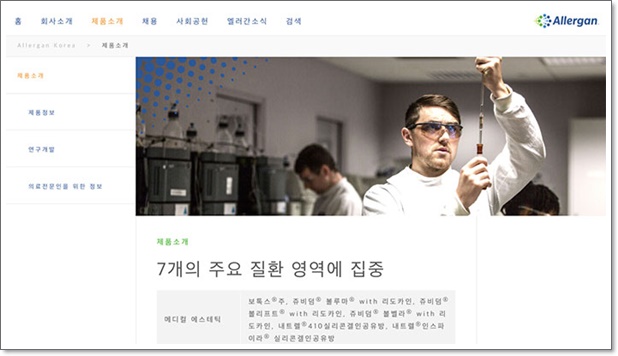
한국과 마찬가지로 미국에서도 엘러간 사 등이 제조한 인공유방 보형물이 많은 여성들의 건강을 해치고 있다.
다음은 ICIJ 국제협업 취재팀이 미국의 인공유방 보형물 피해 실태와 보건 당국의 허술한 관리 문제를 취재한 내용이다.
미국 디트로이트 교외에 사는 로라 디칼란토니오 씨는 유방암 진단을 받고 한 달 후인 2013년 7월, 유방절제술을 받았다. 주치의는 그녀에게 인공유방 보형물을 삽입해 왼쪽 가슴을 재건하길 조언했다.
어린 두 딸을 둔 그녀는 시술 받기가 꺼려졌다. 가슴 실리콘 보형물이 이식 후 새어 나온 사건 때문에 미국 당국이 관련 시술을 10년 넘게 금지시킨 사실이 떠올랐기 때문이다.
보형물이 잘못 될 수 있다는 걱정이 앞섰지만 담당 성형외과의는 보형물 안전성 우려는 옛날 얘기이며, “이것이 할 수 있는 최선의 조치"라고 그녀를 안심시켰다.
디칼란토니오 씨의 경우처럼 인공유방은 유방절제나 사고 이후 가슴을 재건하는 용도로 흔히 사용된다. 미용 목적으로 인공유방 이식을 고려하는 여성도 적지 않다.
그녀는 지난 2013년 12월, 글로벌 의료기기 제조사 엘러간(Allergan)에서 나온 내트렐 스타일 410 실리콘 보형물을 왼쪽 가슴에 삽입하는 시술을 받았다. 이 보형물은 반고체여서 흔히 “곰돌이 젤리(gummy bear)”라고도 불린다.
담당 집도의는 이 제품이 파열되거나 새지 않고 평생 갈 수 있다고 그녀를 안심시켰다. 수술 부위 일부분에 감염 같은 합병증이 있을 수 있다는 얘기는 들었지만 이 제품 자체의 문제나 장기적인 위험성에 대한 경고는 듣지 못했다. 안내는 없었다. 7살과 5살 어린 두 딸을 둔 그녀로서는 회복이 빠르다는 말에 수술을 받기로 결정했다.

디칼란토니오 씨는 수술 뒤 2년은 아무런 문제 없이 건강하게 지냈다. 그러나 2016년 여름부터 알 수 없는 여러가지 증상에 시달리기 시작했다.
왼쪽 팔이 부어올랐고, 림프 부종이라는 진단을 받았다. 입을 완전히 벌리고 닫는 것이 힘든 개구장애도 겪었다. 무릎 뒤에는 체액이 뭉쳐서 발생하는 낭종도 생겼다.
이듬해인 2017년 7월에는 발목 통증으로 족병 전문의를 찾아 물리치료를 받기도 했다. 담당 의사 피터 윌루즈 씨는 ICIJ와의 인터뷰에서 “당시 그녀가 호소하던 통증은 정상적, 전통적인 치료법에 반응하지 않아서 자가면역에 문제가 있는 것 같다고 생각했다"고 말했다.
지난해 12월 디칼란토니오 씨는 인공유방을 이식받은 왼쪽 가슴에 혹을 발견했다. 보형물 파열을 우려한 그녀는 당시 이식 수술을 맡았던 마이클 베닝어 박사를 찾았다.
그녀의 설명에 베닝어 박사는 의심하는 듯 보였고 마지못해 초음파 찍는 것은 동의했다. 그는 진료기록에 “상처이거나 보형물의 일부분인 게 확실해 보이며, 실제 진단보다는 환자 마음의 평화를 위해 초음파를 통해 확인해줄 것임"이라 기록했다.
통증이 그녀의 일상을 집어삼켰다. 체력이 떨어져 자주 지쳤고 통증으로 고통받았으며, 기억력과 집중력이 떨어졌다. 독감에 걸린 듯한 증상 또한 가시질 않았다. 어느 순간에는 통증이 심해 걷기 힘들어지자 집안에 있는 계단을 기어 올라가야 할 정도였다.
가장 힘든 부분은 통증에 시달리느라 체력이 떨어져 아이들과 놀아줄 수 없다는 것이었다.
한때 금지됐던 실리콘 인공유방 … 다시 시장에서 인기
전세계 천만 명의 여성들이 지난 10년 동안 인공유방 이식 수술을 받았다. 심각한 안전성 파문으로 미국에서 장기간 시술 금지됐던 제품이 시장에서 부활한 것이다.
미국 식품의약국(FDA)은 지난 2006년 실리콘 인공유방 시장 판매를 다시 허용하기로 했다. 이는 통상 잘 쓰이지 않는 식염수 인공유방 사용 허가에 뒤이은 결정이다.
이 두 가지 결정의 배경에는 업계 최대 제조사 엘러간과 멘토(Mentor)의 피튀기는 로비전이 있었다. 로비의 목적은 당국에 잦은 제품 파열과 새는 현상, 그리고 이식했던 환자들에게서 보고된 기타 질병들이 옛날 일일 뿐이라고 설득해 시판을 재개하는 것이었다.
그러나 국제탐사언론인협회(ICIJ)의 국제 협업 취재 결과, 처음 실리콘 인공유방이 사용 금지됐을 당시 존재하던 많은 위험성이 현재도 여전히 존재하는 것으로 드러났다.
인공유방 보형물이 자가면역 질환 및 전세계 12명 이상 환자들의 목숨을 앗아간 희귀암과 관련 있다는 연구결과도 늘어나고 있다.
FDA는 안전성 서한에서 제품의 파열과 수축, 그리고 보형물 주변 흉터 조직의 수축으로 인해 인공유방 보형물 이식 수술을 받은 여성 5명 가운데 1명이 수술 10년 안에 보형물을 제거하라고 경고한 바 있다. 인공유방 보형물 이식 수술을 받은 뒤 병에 걸린 여성들의 페이스북 그룹은 회원 수가 5만 명이 넘으며, 매달 수천 명이 늘어나는 추세다.
ICIJ 국제 협업 취재팀이 취재한 바에 따르면 인공유방 보형물에 의한 피해 사례 보고가 늘면서 전세계 보건 당국은 마비 상태이다.
FDA와 업체가 합심해 실리콘 인공유방 제품 위험성 정보 감춰와
다수의 연구 결과에 따르면 인공유방 이식 수술을 받는 대다수의 여성들은 보형물에 만족한다고 보고돼 있다. 이에 대해 FDA는 인공유방 이식 수술의 위험성을 “여성들이 사용 전에 충분히 이해하고 정보에 입각한 결정을 내리는 것”이라고 주장한다.
그러나 ICIJ 국제 협업팀 취재 결과 최근까지 FDA는 인공유방 제조사가 제품 위험성을 일반 대중에게 감출 수 있도록 허용한 것으로 확인됐다.
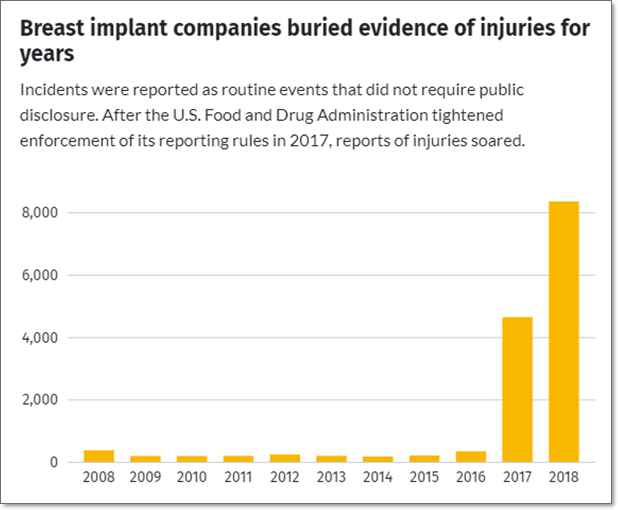
지난 수년 동안 FDA는 제품의 파열과 그 외 손상에 대한 정보를 대중에 공개할 의무가 없는 일상적 사례로 보고하도록 제조사에 허용했다. FDA가 2017년 보고 규정을 강화한 뒤에는 손상 보고가 크게 늘어났으며, 최근 2년 동안의 손상 보고는 그 이전 2년에 비해 20배 넘게 증가했다.
ICIJ가 FDA 이상사례 데이터를 분석한 결과, 인공유방 보형물 손상 의심 사례는 2016년까지 매년 200건도 채 되지 않았다. 그러나 보고 규정 강화 이후 2017년에는 4,567건이 보고됐으며, 2018년에는 상반기에만 8,242건이 보고됐다.
전문가들은 보고 건수가 증가한 것은 인공유방 보형물의 품질이 갑자기 나빠진 것이 아니라 애초부터 안전하지 않았기 때문이라고 말한다.
FDA는 보고받은 실제 손상 건수를 확보하고 있었으나 최근까지 공개하지 않은 것으로 드러났다. 마드리스 톰스 전 FDA 이상사례 데이터 전문 연구원은 “문제는 언제나 상존했다"고 말했다. 톰
스 연구원은 FDA를 퇴사하고 의료기기 이상 사례를 추적하는 ‘디바이스 이벤트'를 설립했다. 그녀는 2017년 회사 데이터베이스를 보다가 처음으로 인공유방 보형물 관련 이상 사례 건수가 급증한다는 점을 포착했다.
ICIJ의 질의에 FDA는 보고 규정이 변경돼 이상 사례 건수가 급증한 것으로 보이는 것이고, 인공유방 제품의 부작용은 새로운 공중 보건 이슈는 아니라고 답변했다.
엘러간 사는 제품이 안전하다는 것은 연구 결과가 증명한다고 주장했다. 엘러간 홍보담당이사 에이미 로즈는 “엘러간의 인공유방 보형물의 안전성은 광범위한 임상 전 기기 시험으로 뒷받침할 수 있으며, 미국과 유럽에서 10년 넘게 진행된 임상 사용과 대규모 연구결과로도 증명할 수 있다"고 답변을 보내왔다.
안전성 보장되지 않아도 잘 나가는 이유 … 허술한 당국의 관리
인공유방 보형물 제조사는 제품 안전성 문제를 해결하지 못한 상태지만 전세계 시장을 지배하고 있다. 이 지배력이 바로 업계가 당국에 영향을 미친다는 증거이며, FDA와 다른 보건 당국이 의료기기 산업 전반을 어떻게 감시하고 있는지에 대해 근본적인 의문을 던지게 한다.
ICIJ 국제협업팀은 당국이 규제를 위반하고, 인공유방 안전성에 대해 제한적으로 또는 잘못된 데이터를 제공한 것에 대해 제조사를 제대로 처벌하지 않았다는 사실을 발견했다.
유럽연합(EU) 보건 당국은 회원국에서 인공유방 보형물 제품을 판매하는 10개 업체 전부가 불충분한 규제 준수 보고서를 제출했지만 계속 영업할 수 있도록 허가했다.
또한 10개 업체 가운데 반 이상은 이식 환자들의 안전성 데이터를 규제에 따라 제대로 추적하지 않았거나, 자사 제품이 인체 조직에 적합한지 증명하는데 실패했다.
미국과 캐나다 규제 당국은 실리콘 인공유방 제품을 다시 시장에 내놓는 조건으로 10년 간 이식 환자들에 대해 추적 연구를 진행하라고 명령했다. 제조사들은 연구 첫 3년도 되지 않아 연구 참여 환자들의 상태를 추적하는 데 실패했지만 정작 당국은 아무런 조치도 취하지 않았다.
전문가들과 환자 단체는 정부가 생명을 위협하거나 그에 준하는 위험성을 기기에 대해 부여하는 ‘블랙박스' 라벨 경고 없이 인공유방 보형물 이식 수술을 허용하고 있어 우려하고 있다.
이들은 당국이 새로운 형태의 암인 ‘유방보형물 관련 역형성대세포림프종(BIA-ALCL)’과 보형물과의 연관성을 증명하는 과학적 증거를 보유하고 있음에도 이 질환을 제대로 다루는 데 실패했다고 주장한다. 이들은 인공유방 보형물이 일으키는 질병과 관련한 새로운 과학적 증거를 제대로 수용하지 않음으로써 여성들을 위험에 빠뜨리고 있다고 말한다.
호주 시드니의 성형외과 의사이자 맥쿼리대 임상의학과 교수 아난드 데바 박사는 “우리는 지금까지 인공유방 보형물 문제를 무시해왔고, 그 결과가 이제 우리에게 자업자득으로 돌아오고 있다"며 “우리는 기하급수적으로 증가하는 합병증을 상대하고 있다"고 말했다.
원인과 해결책 도출 위해서는 업계∙당국의 관리, 활발한 연구가 필요
인공유방 보형물은 통증, 파열, 수축, 감각 상실 등 부분 합병증의 위험성이 크다. ICIJ 취재 결과, 이 같은 질환은 인공유방과 관련해 FDA에 보고되는 질환들 중 가장 흔한 것이다.
‘BIA-ALCL’이라 흔히 알려진 보형물 관련 암은 최근 몇년 간 공중 보건 분야의 관심사로 떠오르고 있다. 성형외과 의사들은 지금까지 전세계에서 570건의 BIA-ALCL 발병 사례를 보고했다. 이 질환은 바깥 쪽 질감이 부드러운 보형물보다는 특별한 질감의 보형물을 이식받은 여성들에게서 훨씬 높게 발생한다.
보건 당국과 성형외과의들은 BIA-ALCL과 인공유방 보형물의 연관성을 폭넓게 인정한 바 있다. 그러나 지금까지 당국은 표면이 특별한 질감을 지닌 보형물 사용에 있어 어떤 제한 조치도 취하지 않았다.
업계와 당국, 성형외과의들은 인공유방 보형물이 자가면역 질환 또는 결합조직 관련 질환을 일으킬 수 있다는 우려를 대부분 예전부터 전해진 신빙성 없는 가설이라며 일축해왔다.
2018년 9월, 미국 휴스턴의 MD 앤더슨암센터 연구진은 인공유방과 관련해 사상 최대, 최장 연구 결과를 발표했다. 이 연구는 실리콘 보형물과 3가지 자가면역 질환의 연관성을 발견했다.
수만 명의 여성들을 관찰한 이스라엘의 한 최근 연구도 이 연관성을 발견했다. 이들 연구는 아직 인공유방 보형물이 왜 이 같은 질환을 야기하는지 규명하지는 못했지만, 통계적으로는 보형물을 이식받은 여성들이 그렇지 않은 여성들 보다는 높은 확률로 자가면역 질환을 호소한다는 점은 보여줬다.
연구자들이 해답을 찾아 나서기 시작했다. 네덜란드 내과 전문의 프라바스 나나야카라 박사는 지난 2008년 폐에 염증이 생긴 환자를 담당하게 됐다. 이 환자의 경우, 이식받은 인공유방 보형물이 새고 있었다. 나나야카라 박사는 어쩌면 보형물이 폐 염증의 원인일 수 있겠다고 추측했다. 이후 박사는 네덜란드 내과 학회에서 해당 케이스를 발표했다.
이후 2013년, 박사는 정식으로 동료 7명과 함께 80명의 인공유방 보형물 이식 환자를 연구했다. 환자 대부분은 보형물 주변 뿐만 아니라 전신에 질환 증세를 나타냈다.
대부분의 환자들이 피로감, 관절 및 근육 통증, 식은땀과 조조경직 등의 증상을 호소했다. 이 가운데 3분의 2 이상은 보형물을 제거한 뒤 증상이 호전됐다.
박사는 보형물에 들어있는 실리콘이 노출되면 체내에서 자가면역 반응을 일으킬 수 있다는 ‘보강제가 유발하는 자가면역 및 염증 신드롬(Autoimmune/inflammatory Syndrome Induced by Adjuvants)' 일명 ‘ASIA 신드롬(ASIA Syndrome)' 가설을 제기했다.
전문가들은 인공유방 보형물과 관련해 장기적인 연구가 더 필요하다고 조언한다. 그러나 엘러겐도 존슨앤드존슨의 유방보형물 브랜드 멘토도 FDA가 4만 명의 이식 환자들을 대상으로 진행하라고 명령한 연구를 이행하지 않았다. 그러나 의무 연구를 이행하지 않고도 두 업체는 아무런 제재도 받지 않았다.
취재: ICIJ 국제협업취재팀 (김지윤, Sasha Chavkin, Emilia Díaz-Struck, Jet Schouten, Rigoberto Carvajal, Amy Wilson-Chapman, Emily Siegel, Madeleine Roy and Razzan Nakhlawi), 정리, 번역 : 김지윤, 일러스트: Christina Chung, ICIJ